Зміст
Повний вступ до технології молекулярно-флуоресцентної візуалізації 5-ALA/ICG в медичній ендоскопії
Молекулярно-флуоресцентна візуалізація – це революційна технологія в галузі медичної ендоскопії останніх років, яка дозволяє досягти точної візуалізації діагностики та лікування в режимі реального часу завдяки специфічному зв'язуванню певних флуоресцентних маркерів (таких як 5-ALA, ICG) з ураженими тканинами. Нижче наведено комплексний аналіз технічних принципів, клінічного застосування, порівняльних переваг, репрезентативних продуктів та майбутніх тенденцій.
1. Технічні принципи
(1) Механізм дії флуоресцентних маркерів
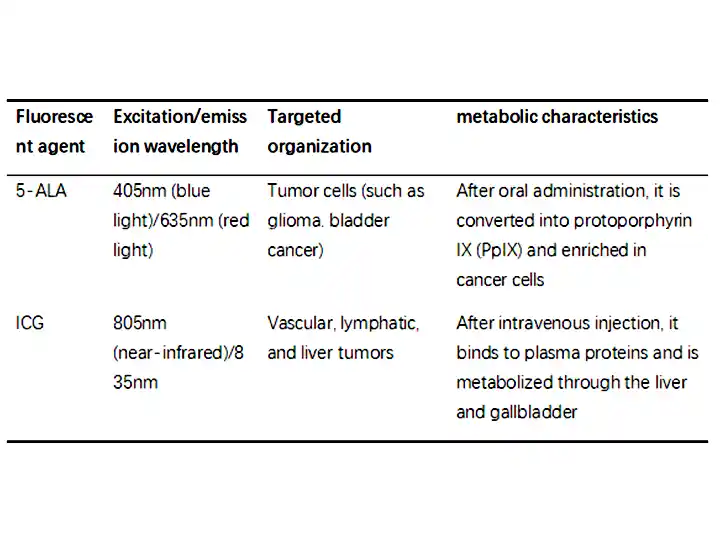
(2) Склад системи візуалізації
Джерело збуджувального світла: світлодіод або лазер із певною довжиною хвилі (наприклад, збудження синім світлом 5-ALA).
Оптичний фільтр: фільтрує інтерференційне світло та фіксує лише флуоресцентні сигнали.
Обробка зображень: накладання флуоресцентних сигналів на зображення білого світла (наприклад, відображення в реальному часі злиття даних системи PINPOINT).
2. Основні переваги (порівняно з традиційною ендоскопією з білим світлом)
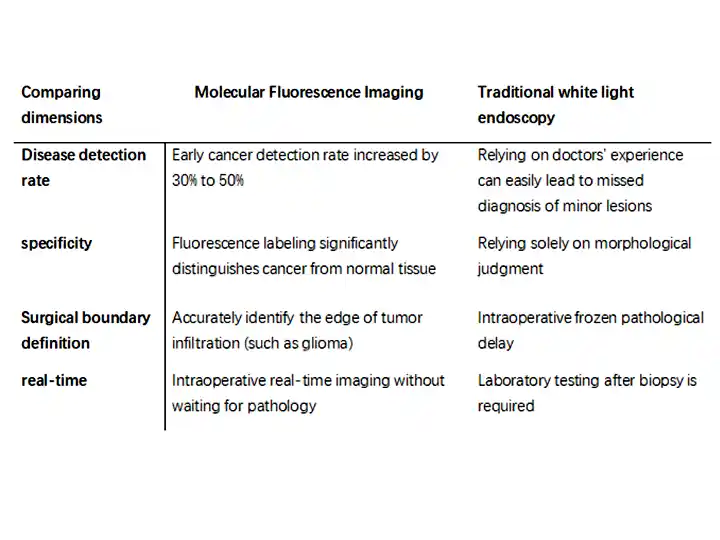
3. Клінічні сценарії застосування
(1) 5-ALA флуоресцентний ендоскоп
Нейрохірургія:
Хірургічна резекція гліоми: флуоресцентне мічення меж пухлини за допомогою PpIX збільшує загальний показник резекції на 20% (якщо схвалено для використання з GLIOLAN).
Урологія:
Діагностика раку сечового міхура: флуоресцентна цистоскопія (наприклад, Karl Storz D-LIGHT C) знижує рівень рецидивів.
(2) Флуоресцентний ендоскоп ICG
Гепатобіліарна хірургія:
Резекція раку печінки: прецизійна резекція ділянок з позитивним затримкою ICG (таких як Olympus VISERA ELITE II).
Хірургія молочної залози:
Біопсія сторожового лімфатичного вузла: трасування ICG замінює радіоактивні ізотопи.
(3) Застосування мультимодального спільного транспорту
Флуоресценція+NBI: Olympus EVIS X1 поєднує вузькосмугову візуалізацію з флуоресценцією ICG для покращення діагностичної частоти раку шлунка.
Флуоресценція+ультразвук: мічення пухлин підшлункової залози за допомогою ІЦГ під контролем ендоскопічного ультразвукового дослідження (ЕУЗД).
4. Представництво виробників та продуктів
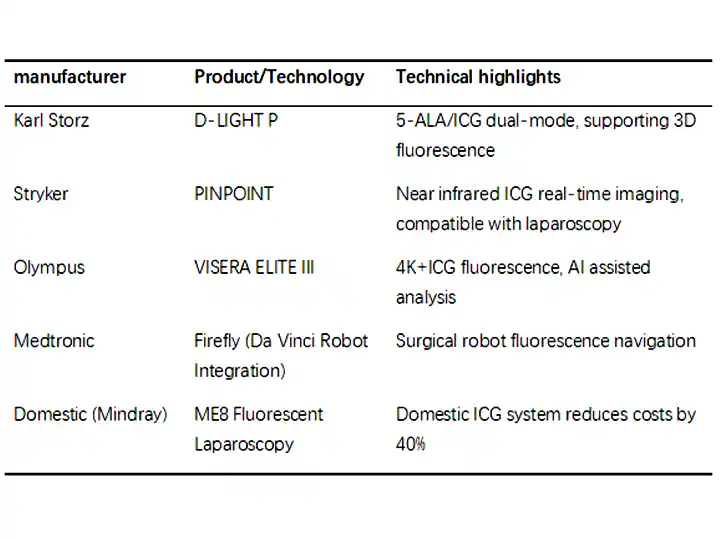
5. Технічні проблеми та рішення
(1) Ослаблення сигналу флуоресценції
Проблема: Тривалість флуоресценції 5-ALA коротка (близько 6 годин).
Рішення:
O Інтраопераційне введення партіями (наприклад, багаторазова перфузія під час операції з приводу раку сечового міхура).
(2) Хибнопозитивний/хибнонегативний
Проблема: Запалення або рубцева тканина можуть помилково розпізнати флуоресценцію.
Рішення:
Мультиспектральний аналіз (наприклад, для розрізнення PpIX та аутофлуоресценції).
(3) Вартість та популяризація
Проблема: Ціна флуоресцентних ендоскопічних систем висока (приблизно від 2 до 5 мільйонів юанів).
Напрямок прориву:
Вітчизняна заміна (наприклад, система Mindray ME8).
Одноразовий флуоресцентний ендоскоп (наприклад, Ambu aScope ICE).
6. Тенденції майбутнього розвитку
(1) Новий флуоресцентний зонд: флуоресцентне мічення пухлинно-специфічними антитілами (наприклад, зонди, спрямовані на EGFR).
(2) Кількісний аналіз за допомогою штучного інтелекту: Автоматизована оцінка інтенсивності флуоресценції (наприклад, використання програмного забезпечення ProSense для оцінки злоякісності пухлини).
(3) Технологія нанофлуоресценції: маркування квантовими точками (КТ) дозволяє здійснювати синхронну візуалізацію кількох цілей.
(4) Портативність: Портативний флуоресцентний ендоскоп (такий, що використовується для скринінгу в лікарнях первинної ланки).
підсумувати
Технологія молекулярно-флуоресцентної візуалізації змінює парадигму діагностики та лікування пухлин завдяки «точному міченню + навігації в режимі реального часу»:
Діагностика: рівень виявлення раку на ранніх стадіях значно зріс, що зменшило кількість непотрібних біопсій.
Лікування: Хірургічний край є точнішим, що знижує ризик рецидиву.
Майбутнє: З диверсифікацією зондів та інтеграцією штучного інтелекту очікується, що він стане стандартним інструментом для «інтраопераційної патології».
Авторське право © 2025. Geekvalue. Усі права захищено.Технічна підтримка: TiaoQingCMS