Spis treści
1、 Rewolucyjny przełom w technologii diagnostycznej
1. Bronchoskopia nawigacyjna elektromagnetyczna (ENB)
Przełomowe: W odpowiedzi na wyzwanie diagnostyczne w zakresie guzków obwodowych płuc (≤ 2 cm) wskaźnik dodatnich wyników biopsji wzrósł z 30% w przypadku tradycyjnej bronchoskopii do ponad 80%.
Technologia podstawowa:
Trójwymiarowa rekonstrukcja TK + pozycjonowanie elektromagnetyczne: np. system nawigacji klatki piersiowej SPiN firmy Veran Medical, który może śledzić położenie instrumentów w czasie rzeczywistym (z błędem mniejszym niż 1 mm).
Kompensacja ruchu oddechowego: SuperDimension™ System eliminuje wpływ przemieszczenia oddechowego poprzez pozycjonowanie 4D.
Dane kliniczne:
Dokładność diagnostyczna guzków płucnych o średnicy 8–10 mm wynosi 85% (badanie Chester 2023).
Połączona szybka ocena cytologiczna na miejscu (ROSE) może skrócić czas operacji o 40%.
2. Bronchoskopia wspomagana robotem
System reprezentatywny:
Platforma Monarch (Auris Health): Elastyczne ramię robota umożliwia sterowanie w zakresie 360°, co pozwala na dotarcie do oskrzeli 8–9 poziomu.
Ion (intuicyjny): ultracienki cewnik o średnicy 2,9 mm i technologii wykrywania kształtu, z dokładnością nakłucia 1,5 mm.
Zalety:
Skuteczność pobierania guzków z górnego płata płuca wzrosła do 92% (w porównaniu do zaledwie 50% w przypadku tradycyjnej mikroskopii).
Zmniejszenie ryzyka wystąpienia powikłań, takich jak odma opłucnowa (wskaźnik zapadalności <2%).
3. Konfokalna endoskopia laserowa (pCLE)
Najważniejsze osiągnięcie techniczne: Sonda Cellvizio ® o średnicy 100 μm umożliwia wyświetlanie struktury pęcherzyków płucnych w czasie rzeczywistym (rozdzielczość 3,5 μm).
Scenariusze zastosowań:
Natychmiastowe różnicowanie pomiędzy nowotworem płuc in situ a atypowym rozrostem gruczolakowatym (AAH).
Ocena patologiczna śródmiąższowej choroby płuc (ILD) in vivo w celu ograniczenia konieczności wykonywania chirurgicznej biopsji płuc.
2. Przełomowe rozwiązania w dziedzinie leczenia
1. Endoskopowa ablacja raka płuc
Ablacja mikrofalowa (MWA):
Dzięki zastosowaniu nawigacji elektromagnetycznej ablacja oskrzeli pozwoliła uzyskać wskaźnik kontroli miejscowej na poziomie 88% (guz ≤ 3 cm, JTO 2022).
W porównaniu do radioterapii: nie stwarza ryzyka zapalenia płuc popromiennego i jest bardziej odpowiednia w przypadku centralnego raka płuc.
Krioablacja:
System Rejuvenair firmy CSA Medical w Stanach Zjednoczonych jest stosowany w celu mroźnej rekanalizacji niedrożności dróg oddechowych.
2. Bronchoplastyka (BT)
Przełomowe: Terapia urządzeniem w leczeniu astmy opornej na leczenie, ukierunkowana na ablację mięśni gładkich.
System Alaira (Boston Scientific):
Trzy operacje zmniejszyły liczbę ostrych ataków astmy o 82% (badanie AIR3).
Zaktualizowane wytyczne z 2023 r. zaleca się dla pacjentów z 5. stopniem GINA.
3. Rewolucja stentu dróg oddechowych
Spersonalizowany wspornik drukowany w technologii 3D:
Na podstawie dostosowanych danych TK rozwiązywanie złożonych zwężeń dróg oddechowych (takich jak zwężenia pogruźlicze).
Przełom materiałowy: Biodegradowalny stent ze stopu magnezu (etap eksperymentalny, całkowite wchłonięcie w ciągu 6 miesięcy).
Stent uwalniający lek:
Stenty pokryte paklitakselem hamują odrost guza (zmniejszając ryzyko restenozy o 60%).
3. Zastosowanie w sytuacjach krytycznych i awaryjnych
1. ECMO połączone z bronchoskopią
Przełom technologiczny:
U pacjentów z zespołem ostrej niewydolności oddechowej (ARDS) wykonuje się płukanie oskrzelowo-pęcherzykowe (BAL) przy użyciu przenośnego ECMO (takiego jak system Cardiohelp).
Weryfikacja bezpieczeństwa operacyjnego u pacjentów ze wskaźnikiem utlenowania <100 mmHg (ICM 2023).
Wartość kliniczna: Określenie patogenu ciężkiego zapalenia płuc i modyfikacja schematu leczenia antybiotykami.
2. Interwencja ratunkowa w przypadku masywnego krwioplucia
Nowa technologia hemostatyczna:
Koagulacja plazmą argonową (APC): bezkontaktowa hemostaza z kontrolowaną głębokością (1-3 mm).
Hemostaza za pomocą sondy zamrażającej: zamknięcie krwawiących naczyń w niskiej temperaturze -40 ℃, wskaźnik nawrotów <10%.
4. Kierunek eksploracji granicznej
1. Endoskopia obrazowa molekularna:
Fluorescencyjne znakowanie przeciwciał PD-L1 (takich jak IMB-134) w celu uwidocznienia w czasie rzeczywistym mikrośrodowiska immunologicznego raka płuc.
2. Nawigacja w czasie rzeczywistym oparta na sztucznej inteligencji:
System Johnson&Johnson C-SATS automatycznie planuje optymalną drogę przepływu powietrza przez oskrzela, co pozwala skrócić czas operacji o 30%.
3. Klaster mikrorobotów:
Magnetyczne mikroroboty MIT potrafią przenosić leki do pęcherzyków płucnych w celu ich uwolnienia.
Tabela porównawcza efektów klinicznych
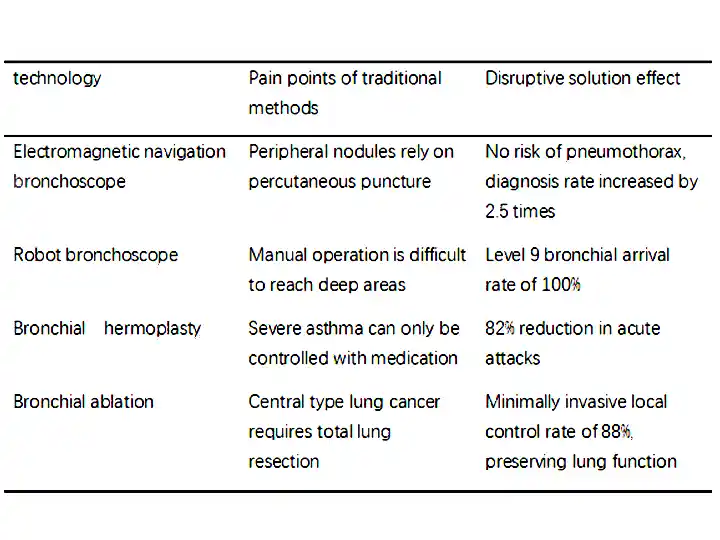
Sugestie dotyczące ścieżki wdrożenia
Szpitale pierwszego kontaktu: wyposażone w bronchoskopię ultrasonograficzną (EBUS) w celu oceny zaawansowania choroby w śródpiersiu.
Szpital trzeciej klasy: Utworzenie centrum interwencji ENB+robot w celu przeprowadzania zintegrowanej diagnostyki i leczenia raka płuc.
Instytucja badawcza: zajmująca się obrazowaniem molekularnym i rozwojem biodegradowalnych rusztowań.
Technologie te zmieniają praktykę kliniczną interwencji oddechowych dzięki trzem przełomowym rozwiązaniom: precyzyjnemu podawaniu leków, inteligentnej diagnostyce i leczeniu ultraminimalnie inwazyjnemu. W ciągu najbliższych 5 lat, dzięki rozwojowi sztucznej inteligencji i nanotechnologii, diagnostyka i leczenie guzków płucnych może osiągnąć poziom „nieinwazyjnego leczenia w obiegu zamkniętym”.
Prawa autorskie © 2025.Geekvalue. Wszelkie prawa zastrzeżone.Wsparcie techniczne: TiaoQingCMS