Spis treści
Niezawodne zaopatrzenie w cystoskopy wspiera wydajność medyczną i dokładność zamówień. Wybór odpowiedniej fabryki cystoskopów gwarantuje stałą jakość, zgodność z przepisami i zaufanie w łańcuchu dostaw.
Szpitale i działy zaopatrzenia w służbie zdrowia często stają przed wyzwaniami związanymi z wyborem fabryki cystoskopów. Od standardów technicznych po modele długoterminowej współpracy, rzetelny producent musi spełniać nie tylko oczekiwania dotyczące produktu, ale także protokoły szpitalne i globalne wymogi regulacyjne. Niniejszy poradnik omawia kluczowe kwestie związane z wyborem kwalifikowanego dostawcy lub producenta cystoskopów i pomaga skutecznie usprawnić proces zaopatrzenia szpitala.
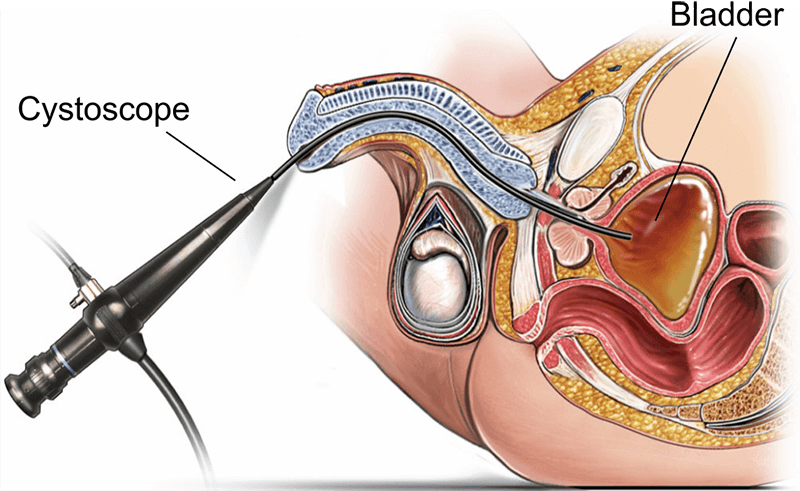
Godna zaufania fabryka cystoskopów charakteryzuje się przestrzeganiem standardów jakości, certyfikatów i transparentnością produkcji. Fabryki produkujące medyczne urządzenia endoskopowe muszą działać zgodnie z surowymi przepisami dotyczącymi wyrobów medycznych. Kluczowe jest, aby produkcja odbywała się w kontrolowanych warunkach, z możliwością śledzenia pochodzenia każdej jednostki, co gwarantuje zgodność z procedurami sterylizacji w szpitalu i protokołami bezpieczeństwa pacjenta.
Oprócz jakości produkcji, kluczową rolę odgrywa doświadczenie fabryki w inżynierii urządzeń medycznych. Długoterminowe zamówienia szpitalne często faworyzują fabryki, które dostarczają pełną dokumentację techniczną, umożliwiają śledzenie partii i oferują stabilne możliwości logistyczne w zakresie dostaw międzynarodowych. Sprawna fabryka cystoskopów zapewnia elastyczność w dostosowywaniu się do indywidualnych potrzeb szpitala, niezależnie od tego, czy chodzi o specyfikacje, złącza, czy kompatybilność z systemami obrazowania.
Cystoskop
Producenci cystoskopów działający na rynkach globalnych muszą spełniać szereg wymogów szpitalnych i regulacyjnych. Obejmuje to normy ISO, oznaczenia CE dla rynków europejskich oraz rejestrację FDA dla szpitali w USA. Jednak sama zgodność nie wystarczy. Producenci muszą również przestrzegać wewnętrznych protokołów, które wspierają produkcję w pomieszczeniach czystych, regularną walidację urządzeń i bieżące audyty jakości.
Wiele szpitali ocenia producentów na podstawie ustrukturyzowanej dokumentacji technicznej i oceny próbek. Jeśli producent może poprzeć zamówienia testowe przejrzystą dokumentacją dotyczącą kompatybilności sterylizacji, instrukcjami konserwacji i dokumentacją dotyczącą gwarancji, często jest postrzegany jako przygotowany do współpracy na poziomie szpitala. Mimo to producenci rzadko są oceniani wyłącznie na podstawie produktu. Ich zdolność do zapewnienia responsywnego wsparcia posprzedażowego często decyduje o długoterminowej wartości.

Dostawca cystoskopów odgrywa kluczową rolę jako pomost logistyczny i komunikacyjny między fabryką a szpitalem. Dla wielu szpitali, zwłaszcza tych spoza regionu producenta, bezpośrednia współpraca z dostawcą cystoskopów, który zna lokalne przepisy, logistykę wysyłkową i protokoły użytkowania, zapewnia sprawniejszy proces zaopatrzenia.
Skuteczni dostawcy dostarczają zespołom zaopatrzeniowym dokładne prognozy dostępności, szczegółowe listy pakowania, wytyczne dotyczące sterylizacji oraz dokumentację importową. Szpitale często proszą dostawców o koordynację certyfikatów kalibracji, testów przed wysyłką i posprzedażowego wsparcia technicznego. Usługi te pomagają działom zaopatrzenia ograniczyć niepewność i usprawnić integrację z istniejącymi systemami endoskopowymi.
Co więcej, zdolność dostawcy do reagowania na zapytania techniczne i prośby o wymianę sprzętu wpływa na przepływ pracy w szpitalu. W przypadku powtarzających się zamówień hurtowych, responsywny dostawca staje się niezbędny. Dlatego niezawodność komunikacji i dokumentacji jest równie ważna, jak jakość samego urządzenia.
Nowoczesne szpitale często poszukują rozwiązań niestandardowych, dostosowanych do demografii pacjentów, potrzeb proceduralnych lub systemów wewnętrznych. Nowoczesna fabryka cystoskopów jest przygotowana na realizację takich zamówień bez zakłócania harmonogramów produkcji.
Niezależnie od tego, czy chodzi o dostosowanie długości rurki intubacyjnej, integrację źródeł światła LED, czy modyfikację uchwytów pod kątem ergonomii, fabryki oferujące produkcję modułową są preferowane przez zespoły zaopatrzeniowe. Dostosowania obejmują również etykietowanie, formaty opakowań i kompatybilność ze sterylizacją w poszczególnych regionach.
Możliwość personalizacji pozwala szpitalom na dostosowanie urządzeń do protokołów chirurgicznych i systemów przechowywania. Wspiera również środowiska szkoleniowe, w których standardowe narzędzia pomagają zespołom medycznym ćwiczyć z precyzją.
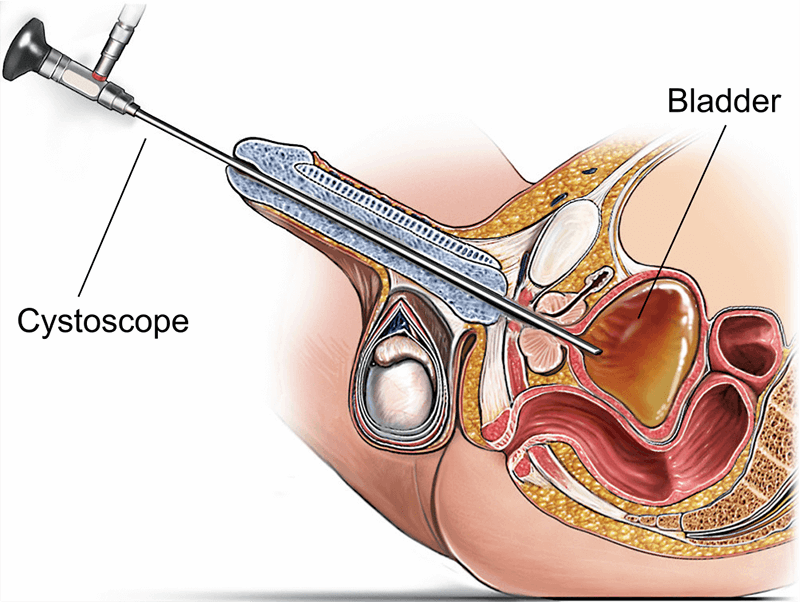
Identyfikowalność jest kluczowa zarówno dla zapewnienia jakości, jak i zgodności z przepisami. Producenci cystoskopów muszą prowadzić dzienniki produkcji dla poszczególnych urządzeń, od pozyskiwania materiałów po końcową sterylizację. Szpitale często wymagają etykietowania seryjnego, kodów kreskowych i dokumentacji cyfrowej, aby dostosować je do wewnętrznych systemów śledzenia urządzeń.
Wiarygodny producent integruje identyfikowalność nie tylko jako krok w kierunku zapewnienia jakości, ale jako rutynową praktykę. Dzięki śledzeniu w chmurze wiele fabryk może teraz zapewnić szpitalom wgląd w czasie rzeczywistym w status zamówień i etapy produkcji. Minimalizuje to opóźnienia i buduje transparentność w długoterminowych partnerstwach.
Globalne systemy opieki zdrowotnej różnią się pod względem przepisów, języka i procedur celnych. Dostawca cystoskopów dostosowany do rynków międzynarodowych to taki, który zapewnia wielojęzyczną dokumentację, doświadczenie w zakresie wysyłek międzynarodowych i znajomość certyfikatów.
Poza tym międzynarodowi dostawcy często zajmują się specyficznymi wymaganiami szpitali, takimi jak kompatybilność z podwójnym napięciem urządzeń do obrazowania czy regionalne standardy sterylizacji. Terminowa dostawa ma kluczowe znaczenie, zwłaszcza gdy szpitale koordynują operacje lub otwierają nowe oddziały w oparciu o dostarczony sprzęt.
Dobrzy dostawcy przewidują również pytania ze strony szpitali, zanim się pojawią. Może to obejmować dostarczanie filmów instruktażowych, instrukcji obsługi dostosowanych do języków regionalnych lub oferowanie telepomocy w zakresie instalacji i szkoleń.
Cena cystoskopu zależy od kilku czynników, takich jak złożoność konstrukcji, jakość obrazowania, możliwość ponownego użycia oraz struktura dostawców. Podstawowe cystoskopy wielokrotnego użytku mogą być bardziej przystępne cenowo, ale ich długotrwałe użytkowanie wymaga inwestycji w sterylizację i konserwację.
Systemy wysokiej klasy ze zintegrowanymi kamerami, zaawansowanym oświetleniem lub łącznością bezprzewodową są droższe i zazwyczaj kupują je szpitale trzeciego stopnia referencyjności. Cystoskopy jednorazowego użytku są coraz powszechniejsze na oddziałach o dużej przepustowości, co ma na celu ograniczenie ryzyka zakażeń, choć ich cena jednostkowa jest wyższa.
Dodatkowo, zakup cystoskopu za pośrednictwem dostawcy może wiązać się z kosztami logistycznymi, dokumentacją i opłatami podatkowymi. Szpitale często porównują koszty początkowe z jakością usług i długoterminową niezawodnością dostawcy.
Cystoskop to fizyczne urządzenie medyczne – narzędzie endoskopowe wprowadzane przez cewkę moczową w celu uwidocznienia pęcherza moczowego. Obejmuje ono elementy optyczne, oświetleniowe i wprowadzające. Cystoskopia to natomiast zabieg kliniczny, w którym używa się cystoskopu.
Zrozumienie tej różnicy jest ważne dla zespołów zaopatrzeniowych. Szpitale kupują cystoskopy, ale zakupy te są powiązane z obsługą procedur cystoskopii, które różnią się w zależności od potrzeb diagnostycznych lub interwencyjnych. Dlatego konstrukcja urządzenia musi spełniać oczekiwania proceduralne zespołu medycznego, w tym kompatybilność z systemami irygacyjnymi, narzędziami do biopsji lub światłowodami laserowymi.
Cystoskop
Zamówienia szpitalne rzadko dotyczą pojedynczych transakcji. Zamiast tego, to ciągła relacja kształtowana przez niezawodność dostaw, udoskonalenia techniczne i responsywne wsparcie. Producenci cystoskopów, którzy stale inwestują w udoskonalanie produktów, automatyzację produkcji i kanały informacji zwrotnej po wprowadzeniu produktu na rynek, są często faworyzowani przez systemy szpitalne dążące do utrzymania stałej jakości przez długi czas.
Długoterminowa współpraca usprawnia również wprowadzanie nowych produktów, umożliwiając szpitalom wdrażanie ulepszeń lub innowacji bez konieczności ponownej walidacji całego łańcucha dostaw. Zwłaszcza w regionach charakteryzujących się szybkim postępem technologicznym lub zmianami regulacyjnymi, takie partnerstwa zapewniają ciągłość operacyjną.
Oceniając fabrykę cystoskopów, specjaliści ds. zaopatrzenia szpitali muszą znaleźć równowagę między możliwościami produkcyjnymi, zgodnością z przepisami, jakością usług i elastycznością. Podobnie producenci i dostawcy muszą spełniać globalne oczekiwania w zakresie opieki zdrowotnej poprzez ustrukturyzowaną dokumentację i dostosowanie techniczne.
W przypadku szpitali poszukujących długoterminowego, stabilnego źródła zaopatrzenia w sprzęt endoskopowy i obrazowy, współpraca z doświadczonymi firmami w branży zapewnia spójność opieki nad pacjentem i wydajność procedur.
XBX, jako marka specjalizująca się w dziedzinie endoskopów medycznych, wspiera szpitale i dystrybutorów na całym świecie, oferując profesjonalne rozwiązania produkcyjne i dostawcze przeznaczone do zastosowań klinicznych.
Szpitale powinny weryfikować system jakości fabryki cystoskopów nie tylko na podstawie certyfikatów, ale także poprzez weryfikację rzeczywistej realizacji, dyscypliny CAPA, kontroli dostawców, zarządzania ryzykiem i identyfikowalności. Dzięki temu będą współpracować z niezawodnymi producentami cystoskopów i niezawodnymi dostawcami cystoskopów.
Wiarygodna fabryka cystoskopów to dowód, a nie tylko papierkowa robota. Certyfikaty mają znaczenie, ale zespoły zaopatrzeniowe muszą mieć wgląd w systemy, które zapewniają jakość na co dzień. Doświadczeni producenci cystoskopów prowadzą aktualną, kontrolowaną dokumentację i weryfikowalną dokumentację, która pokazuje, jak organizacja przekształca procedury w spójne rezultaty.
Rejestry ECR/ECO śledzą zmiany w projekcie i umożliwiają zatwierdzanie zmian międzyfunkcyjnych.
Zweryfikowane procesy (IQ/OQ/PQ) dotyczące ustawiania optycznego, montażu sekcji gięcia i testowania szczelności.
Rutynowe punkty kontrolne w trakcie procesu powiązane z kryteriami akceptacji i planami reakcji.
Dostęp do najnowszych procedur operacyjnych (SOP) na poziomie hali produkcyjnej; przestarzałe wersje są archiwizowane i niedostępne.
Gdy te artefakty są kompletne, opatrzone datą i można je powiązać z partiami i numerami seryjnymi, szpitale mogą zaufać dojrzałości operacyjnej dostawcy cystoskopów, a nie tylko ścianie certyfikatów.
Skuteczny program CAPA ujawnia kulturę. Jeśli skargi na wycieki się kumulują, fabryka cystoskopów powinna zidentyfikować ich pierwotne przyczyny – okna czasowe utwardzania kleju, zmienność uszczelek typu O-ring, technikę operatora – a następnie wdrożyć działania korygujące i zapobiegawcze, zweryfikować ich skuteczność i zamknąć je na czas. Zastosowanie metody „5 Why” i metody „rybiej ości” z jasno określonymi prawami własności pokazuje, że dostawca cystoskopów traktuje problemy jako okazje do poprawy, a nie do ukrycia.
Zdefiniowano czynniki wyzwalające CAPA i ustalono priorytety na podstawie ryzyka.
Dowody wskazujące na przyczynę problemu, a nie założenia.
Kontrole skuteczności przy użyciu mierzalnych kryteriów i terminów.
Eskalacja kierownictwa w przypadku opóźnionych działań.
Szpitale powinny dokonać przeglądu bazy danych skarg i planu nadzoru po wprowadzeniu produktu na rynek. Solidni producenci cystoskopów monitorują trendy drobnych sygnałów, śledzą zewnętrzne komunikaty dotyczące nadzoru i przeprowadzają symulacje wycofania produktu, aby sprawdzić gotowość. W przypadku wycofania produktu, harmonogram reakcji, jakość dokumentacji i komunikacja z organami regulacyjnymi wskazują, jak dostawca cystoskopu radzi sobie pod presją.
Powiązanie skargi, partii i serii z notatkami z dochodzenia.
Wykresy trendów i progi uruchamiające CAPA.
Udokumentowane pozorowane wycofania produktów z metrykami czasu potrzebnego do ich śledzenia.
Kontrola dokumentacji musi być zgodna z zasadami ALCOA. Operatorzy w fabryce cystoskopów powinni mieć dostęp wyłącznie do najnowszych procedur operacyjnych (SOP). Rejestry partii – elektroniczne lub papierowe – muszą być aktualne, czytelne i możliwe do przypisania, z zachowaniem ścieżek audytu i zgodnymi z przepisami podpisami elektronicznymi. Zapobiega to wprowadzaniu danych po fakcie i zwiększa zaufanie do wyników raportowanych przez dostawcę cystoskopu.
Ponieważ czujniki, optyka, precyzyjne przewody i biokompatybilne kleje pochodzą z globalnej sieci, producenci cystoskopów potrzebują solidnej kwalifikacji dostawców i kontroli jakości dostaw. Kluczowe części mogą wymagać 100% kontroli; inne powinny korzystać z próbkowania opartego na AQL. Podwójne źródła zaopatrzenia i karty wyników dostawców (wskaźnik odrzuceń, terminowość dostaw, responsywność CAPA) pokazują, czy fabryka cystoskopów jest w stanie wytrzymać wstrząsy bez uszczerbku dla niezawodności.
Ustrukturyzowane wdrażanie dostawców i okresowe audyty.
Certyfikaty materiałowe i możliwe do prześledzenia wyniki kontroli.
Jasne zasady postępowania w przypadku niezgodności i oczekiwania CAPA wobec dostawców.
Pliki ryzyka zgodne z normą ISO 14971 powinny być dokumentami „na żywo”. Zagrożenia takie jak zakażenia krzyżowe, wycieki czy rozbieżności optyczne muszą być powiązane z weryfikowanymi i walidowanymi mechanizmami kontroli ryzyka. W przypadku reklamacji, niezawodni producenci cystoskopów przekazują informacje do pliku ryzyka i ponownie oceniają ryzyko resztkowe. Ta zamknięta pętla dowodzi, że dostawca cystoskopu zarządza rzeczywistymi informacjami zwrotnymi, a nie tylko raz przechodzi audyt.
Ludzie sprawiają, że jakość staje się rzeczywistością. Fabryka cystoskopów powinna utrzymywać matryce szkoleniowe, certyfikować operatorów do wykonywania kluczowych zadań (ustawianie optyczne, nakładanie kleju, testowanie szczelności) i planować ponowną certyfikację. Podczas audytów należy prosić operatorów o wyjaśnienie kluczowych kroków; pewne, spójne odpowiedzi często odróżniają czołowych producentów cystoskopów od tych, którzy dysponują jedynie dokumentacją papierową.
Każde urządzenie powinno być identyfikowalne od surowca do końcowego testu. Wiarygodny dostawca cystoskopów przypisuje unikalne numery seryjne lub kody UDI, które Twój szpital może zeskanować. Wybierz losowo gotowy endoskop i poproś o pełną dokumentację – identyfikatory sprzętu, parametry procesu, wyniki kontroli i potwierdzenia odbioru. Fabryka cystoskopów, która pobiera te dane w ciągu kilku minut, zazwyczaj prowadzi elektroniczne rejestry partii z bezpiecznymi ścieżkami audytu, co jest silnym czynnikiem predykcyjnym gotowości do wycofania produktu.
Powiązanie partii z komponentami, aż do kluczowych dostawców.
Dane testowe przechowywane są ze znacznikami czasu i identyfikatorami operatorów.
Oznakowanie UDI jest zgodne z przepisami regionalnymi.
Poproś o wgląd do programu audytu wewnętrznego: kalendarza, kwalifikacji audytorów, ustaleń i zamknięć. Protokoły z przeglądów kierownictwa powinny zawierać informacje o celach jakościowych, trendach w zakresie reklamacji, statusie CAPA oraz alokacji zasobów. Kiedy kierownictwo fabryki cystoskopów uczestniczy w tych przeglądach i ogłasza budżet lub stan zatrudnienia w celu rozwiązania problemów, dowiadujesz się, że jakość ma charakter strategiczny – jest to cecha charakterystyczna dla odpowiedzialnych producentów cystoskopów.
Stoły optyczne, testery szczelności, mierniki momentu obrotowego i komory środowiskowe muszą być zgodne z harmonogramami kalibracji, zgodnymi z normami krajowymi. Jeśli instrument przekroczy dopuszczalną tolerancję, dostawca cystoskopu powinien poddać kwarantannie potencjalnie wadliwy produkt, przeprowadzić analizę wpływu i udokumentować podjęte działania. Ta dyscyplina metrologiczna zapobiega niezauważalnym zmianom w działaniu produktu.
Cystoskopy są wrażliwe na kurz, wilgoć i temperaturę. Wiarygodna fabryka cystoskopów utrzymuje kontrolowane strefy (często klasy ISO 7 dla optyki), rejestruje liczbę cząstek i kontroluje parametry środowiskowe wpływające na utwardzanie kleju i stabilność polimerów. Przepływ materiału oddziela strefy czyste od brudnych, a procedury zakładania fartuchów są egzekwowane – nawyki powszechne wśród wiodących producentów cystoskopów.
Poza zgodnością, szukaj sygnałów organizacji uczącej się: wykresów SPC dla kluczowych parametrów, paneli wydajności pierwszego przejścia, wydarzeń Kaizen eliminujących marnotrawstwo oraz projektów Six Sigma ukierunkowanych na chroniczne defekty. Kiedy dostawca cystoskopów wykazuje roczne skrócenie czasu przeróbek i realizacji, zyskujesz pewność, że dzisiejsze dobre wyniki będą jeszcze lepsze jutro.
Jeśli fabryka cystoskopów korzysta z elektronicznego systemu zarządzania jakością (QMS), należy potwierdzić kontrolę dostępu, tworzenia kopii zapasowych, odzyskiwania danych po awarii i śledzenia audytu. W obliczu rosnących zagrożeń cybernetycznych ochrona danych jakościowych jest elementem integralności produktu. Doświadczeni producenci cystoskopów mogą opisać, jak testują odtworzenia i jak szybko są w stanie odzyskać dane po incydencie cybernetycznym.
Zgodnie z unijnymi przepisami MDR i przepisami FDA QSR wymagania ewoluują. Zapytaj, jak dostawca cystoskopów prowadzi działania PMCF/PMR, aktualizuje dokumentację techniczną i przygotowuje się do inspekcji. Przejrzystość historii inspekcji – oraz terminowe, udokumentowane odpowiedzi – świadczą o tym, że fabryka cystoskopów jest pewna swojego systemu i uczciwa wobec partnerów.
Jeśli to możliwe, przeprowadź symulację wycofania produktu z rynku lub symulację audytu. Najlepsi producenci cystoskopów potrafią zidentyfikować wadliwe partie w ciągu kilku godzin i przedstawić wersje robocze powiadomień oraz wnioski regulacyjne. Obserwowanie dostawcy cystoskopów pod presją czasu to jeden z najszybszych sposobów oceny gotowości do działania w warunkach rzeczywistych.
Dogłębna analiza pomaga szpitalom oddzielić twierdzenia marketingowe od faktów operacyjnych. Fabryka cystoskopów, która dokumentuje rzeczywiste wdrożenie, zamyka CAPA, kontroluje dostawców i stale się rozwija, będzie chronić pacjentów i budżety. Wybór takich producentów cystoskopów przekształca proces zaopatrzenia w stabilną, opartą na danych współpracę – dokładnie taką, jaką powinien oferować niezawodny dostawca cystoskopów.
Wiarygodna fabryka cystoskopów powinna posiadać certyfikat ISO 13485, rejestrację FDA oraz zgodność z CE/MDR. Certyfikaty te potwierdzają, że producent stosuje uznane na całym świecie systemy zarządzania jakością dla wyrobów medycznych.
Wiodący producenci cystoskopów stosują sprawdzone procesy (IQ/OQ/PQ), statystyczną kontrolę procesu oraz automatyczne testy szczelności. Każda partia przechodzi końcową kontrolę jakości, aby zagwarantować stałą przejrzystość optyczną, odporność na zginanie i bezpieczeństwo pacjenta.
Tak. Odpowiedzialny dostawca cystoskopów prowadzi dzienniki działań korygujących i zapobiegawczych (CAPA), które dokumentują analizę przyczyn źródłowych, działania korygujące, kroki zapobiegawcze i weryfikację zamknięcia każdej niezgodności.
Szpitale powinny poprosić o demonstrację, w ramach której fabryka cystoskopów pobierze pełną genealogię losowego urządzenia, w tym surowce, identyfikatory operatorów, użyty sprzęt i wyniki inspekcji. To dowodzi skutecznej identyfikowalności i gotowości do obsługi UDI.
Zaufani producenci cystoskopów przeprowadzają audyty dostawców, egzekwują kontrole jakości dostaw z uwzględnieniem zdefiniowanych wskaźników AQL i prowadzą karty wyników wydajności. Podwójne pozyskiwanie kluczowych komponentów, takich jak czujniki obrazu, również zmniejsza ryzyko związane z zaopatrzeniem.
Kompetentny dostawca cystoskopów dostarcza dokumentację techniczną, dokumentację zarządzania ryzykiem, raporty z oceny klinicznej oraz dane z nadzoru po wprowadzeniu do obrotu. Dokumenty te pomagają szpitalom wykazać zgodność z przepisami podczas inspekcji regulacyjnych.
Prawa autorskie © 2025.Geekvalue. Wszelkie prawa zastrzeżone.Wsparcie techniczne: TiaoQingCMS